Introduction aux solutions électrolytiques
Une solution électrolytique est une solution capable de conduire le courant électrique. Cette propriété est due à la présence d’ions, des particules chargées qui se déplacent librement dans le liquide. Dans ce cours destiné aux élèves de 1ère Bac Sciences, vous allez découvrir comment ces solutions se forment, les étapes de la dissolution et comment calculer les différentes concentrations.
Qu’est-ce qu’un corps solide ionique ?
Un solide ionique est un composé chimique formé d’ions positifs, appelés cations, et d’ions négatifs, appelés anions. Ces ions sont arrangés de manière régulière et ordonnée dans une structure tridimensionnelle solide, que l’on nomme un cristal. L’ensemble du solide est électriquement neutre, car la somme des charges positives des cations compense exactement la somme des charges négatives des anions. Le sel de table, ou chlorure de sodium (NaCl), est un exemple parfait de solide ionique, constitué d’ions Na⁺ et Cl⁻.
Le caractère dipolaire d’une molécule
Pour comprendre pourquoi l’eau est un si bon solvant, il faut s’intéresser à la polarité des molécules.
Liaison covalente et électronégativité
Une liaison covalente se forme lorsque deux atomes mettent en commun des électrons. L’électronégativité est la capacité d’un atome à attirer vers lui les électrons de cette liaison.
Dans une molécule comme celle de l’eau (H₂O), l’atome d’oxygène est beaucoup plus électronégatif que les atomes d’hydrogène. Il attire donc plus fortement les électrons des liaisons, ce qui crée :
- Un pôle avec une charge partielle négative (δ-) du côté de l’oxygène.
- Des pôles avec des charges partielles positives (δ+) du côté des hydrogènes.
Cette séparation des charges fait de la molécule d’eau une molécule polaire, ou un dipôle. C’est cette polarité qui lui permet d’interagir fortement avec les ions.
Le processus de dissolution d’un électrolyte
Lorsqu’on dissout un composé ionique (le soluté) dans l’eau (le solvant), trois étapes se succèdent pour former une solution électrolytique.
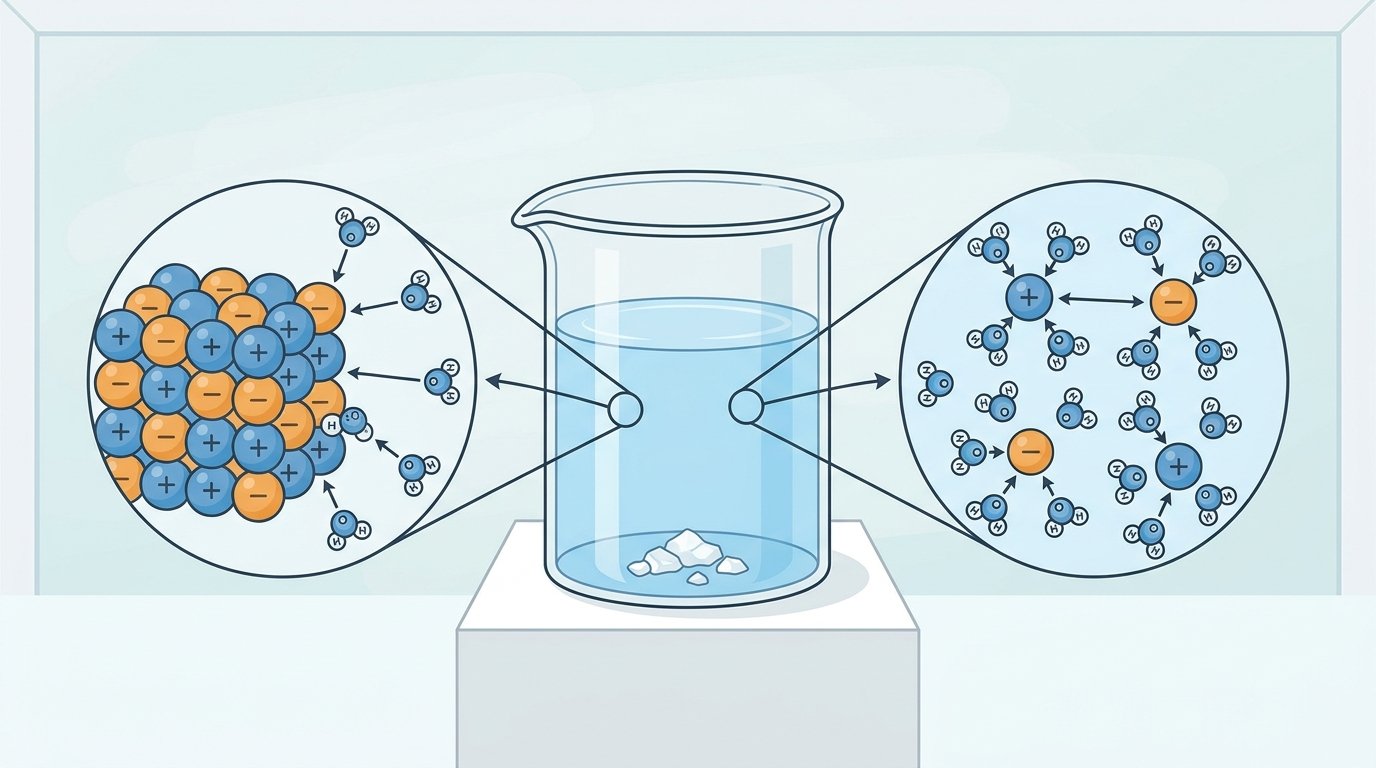
- La dissociation : Les molécules d’eau polaires entourent le cristal. Leur attraction est assez forte pour briser les liaisons du cristal et séparer les cations des anions.
- La solvatation (ou hydratation) : Une fois libérés, les ions sont immédiatement entourés par des molécules d’eau. Le pôle négatif de l’eau s’oriente vers les cations (positifs), et les pôles positifs s’orientent vers les anions (négatifs). Quand le solvant est l’eau, on parle d’hydratation.
- La dispersion : Les ions hydratés, désormais libres de se déplacer, se répartissent de manière uniforme dans toute la solution. C’est la présence de ces ions mobiles qui permet à la solution de conduire l’électricité.
L’équation de la réaction de dissolution
On modélise la dissolution par une équation chimique qui montre le soluté initial se transformant en ions en solution aqueuse. Il est crucial d’indiquer l’état physique de chaque espèce : (s) pour solide, (l) pour liquide, (g) pour gaz et (aq) pour aqueux (dissous dans l’eau).
Exemples :
- Dissolution du chlorure de sodium (solide) : NaCl(s) → Na⁺(aq) + Cl⁻(aq)
- Dissolution du chlorure d’hydrogène (gaz) : HCl(g) → H⁺(aq) + Cl⁻(aq)
Calcul des concentrations molaires
En chimie, il est essentiel de quantifier les espèces présentes dans une solution. On utilise pour cela les concentrations molaires.
Concentration molaire du soluté (C)
La concentration molaire d’un soluté apporté, notée C, représente la quantité de matière (n) de soluté dissoute par litre de solution (V). Elle s’exprime en moles par litre (mol·L⁻¹).
La formule est : C = n / V
Concentration molaire effective des ions [X]
La concentration molaire effective, notée avec des crochets [X], est la concentration réelle d’une espèce ionique X présente dans la solution. Elle se calcule de la même manière.
La formule est : [X] = n(X) / V
Relation entre les concentrations
Les concentrations effectives des ions dépendent directement de la concentration du soluté C et des coefficients stœchiométriques de l’équation de dissolution.
Prenons l’exemple de la dissolution du chlorure de calcium, CaCl₂ :
CaCl₂(s) → Ca²⁺(aq) + 2Cl⁻(aq)
Si la concentration en soluté apporté est C, alors les concentrations effectives des ions sont :
- [Ca²⁺] = 1 × C = C
- [Cl⁻] = 2 × C
La concentration des ions chlorure est donc le double de celle du soluté apporté, car chaque mole de CaCl₂ libère deux moles d’ions Cl⁻.
Liens utiles
Pour vous entraîner sur ce chapitre, passez directement à notre série d’exercices sur la concentration et les solutions électrolytiques.
Explorez d’autres cours et exercices de chimie dans notre rubrique 1ère Année Baccalauréat.