Introduction aux dosages directs
Un dosage, aussi appelé titrage, est une technique d’analyse chimique essentielle qui permet de déterminer la concentration molaire inconnue d’une espèce chimique dissoute dans une solution. Pour cela, on fait réagir cette solution avec une autre solution de concentration parfaitement connue. C’est une méthode précise et couramment utilisée en laboratoire, par exemple pour des analyses sanguines ou le contrôle qualité de produits.
Principe du dosage direct
Le principe repose sur une réaction chimique entre deux solutions :
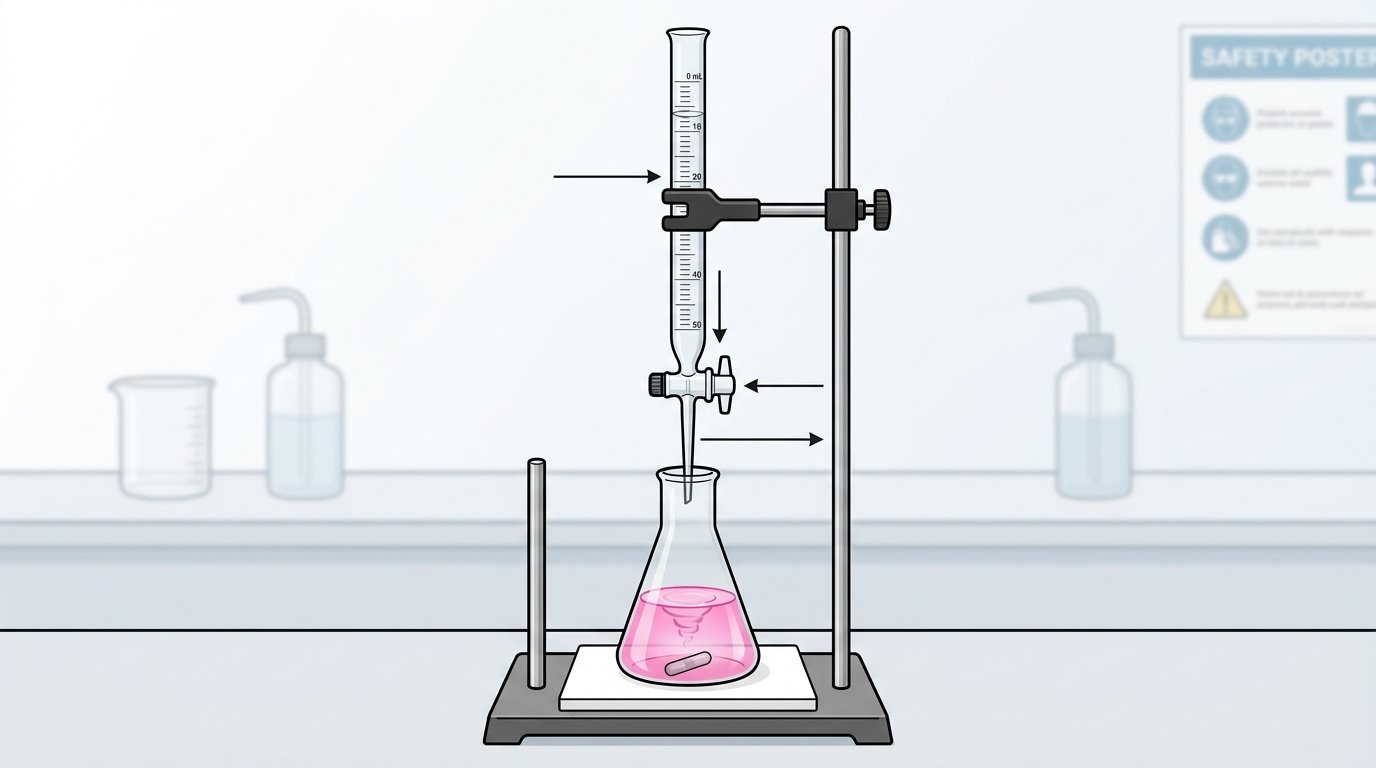
- La solution titrée : c’est la solution contenant l’espèce chimique dont on cherche la concentration. Elle est généralement placée dans un bécher ou un erlenmeyer.
- La solution titrante : c’est la solution de concentration connue qui va réagir avec l’espèce à doser. Elle est placée dans une burette graduée.
On verse progressivement la solution titrante dans la solution titrée jusqu’à ce que la réaction soit complète. Ce moment précis s’appelle l’équivalence.
Les conditions d’une réaction de dosage
Pour qu’un dosage soit valide, la réaction chimique utilisée doit respecter trois conditions fondamentales :
- Univoque (ou unique) : Les réactifs titrant et titré ne doivent réagir que selon une seule réaction chimique, sans réactions secondaires.
- Totale : La réaction doit être complète. L’un des réactifs doit être entièrement consommé.
- Rapide : La réaction doit être instantanée pour que l’on puisse observer l’équivalence dès qu’elle est atteinte.
L’équivalence : Le point clé du dosage
Définition de l’équivalence
L’équivalence est le moment du dosage où les réactifs (l’espèce titrée et l’espèce titrante) ont été mélangés dans les proportions stœchiométriques de l’équation de la réaction. À ce point précis, les deux réactifs sont entièrement consommés. Il y a un changement de réactif limitant.
Comment repérer le point d’équivalence ?
L’objectif principal d’un dosage expérimental est de repérer précisément ce point d’équivalence. On peut le faire de plusieurs manières :
- Changement de couleur (dosage colorimétrique) : C’est la méthode la plus visuelle. Soit l’un des réactifs ou produits est naturellement coloré (comme le permanganate de potassium), soit on ajoute quelques gouttes d’un indicateur coloré spécifique qui change de couleur au voisinage de l’équivalence.
- Suivi d’une grandeur physique : On peut suivre l’évolution continue d’une grandeur physique de la solution pendant l’ajout du réactif titrant. Par exemple, on peut mesurer la conductance G (dosage conductimétrique) ou le pH (dosage pH-métrique). L’équivalence est alors repérée graphiquement par un changement de pente brutal sur la courbe tracée.
La relation à l’équivalence
Soit l’équation de la réaction de dosage : a A + b B → produits
- A est l’espèce titrée (de concentration CA inconnue, et de volume VA connu).
- B est l’espèce titrante (de concentration CB connue, et dont le volume versé à l’équivalence est VBE).
À l’équivalence, les réactifs A et B ont été introduits dans les proportions stœchiométriques. On peut donc écrire la relation fondamentale suivante, basée sur les quantités de matière (n) :
nA / a = nB(versé) / b
En remplaçant la quantité de matière par le produit de la concentration et du volume (n = C × V), la relation devient :
(CA × VA) / a = (CB × VBE) / b
Cette équation est la clé du dosage. Elle permet de calculer mathématiquement la concentration inconnue CA une fois le volume à l’équivalence VBE déterminé expérimentalement.
Liens utiles
Pour vous entraîner sur ce chapitre, passez à notre série d’exercices sur les dosages directs.
Retrouvez tous nos cours et exercices de chimie pour la 1ère Année Baccalauréat.